
脳梗塞と高尿酸血症
平野 照之 先生
杏林大学医学部脳卒中医学教室 教授
高尿酸血症は脳卒中のリスク因子となるか?
高尿酸血症では血清尿酸値が高くなっていく過程で酸化ストレスを生じ、この酸化ストレスが血管を傷つけることで動脈硬化を促し、心筋梗塞や脳梗塞、腎機能低下などの組織障害を誘導する。理論的に矛盾のないストーリーではあるが、臨床的なエビデンスには乏しい。実際、『脳卒中治療ガイドライン2021〔改訂2023〕』1)では、脳卒中のリスク因子として高血圧、糖尿病、脂質異常症、飲酒・喫煙、心疾患、肥満・メタボリックシンドローム、慢性腎臓病などがリストアップされ具体的な介入を推奨しているが、そこに血清尿酸値の記載はない。それゆえ、脳卒中に携わる医師にとって高尿酸血症は漠然としたリスク因子としての認識に留まっている。ただ、最近では心原性脳塞栓症の原因の多くを占める心房細動の一要因として、高尿酸血症が関わっているとの見解もある。
脳梗塞の疫学
わが国の脳卒中疫学を経年的にみた『脳卒中データバンク2021』2)によると、近年の脳梗塞の病型別頻度は、アテローム血栓性脳梗塞が31.5%、心原性脳塞栓症が28.8%、ラクナ梗塞が28.2%、その他が約10%程度と報告されている(図1A)。
心原性脳塞栓症は心房細動などの不整脈を主な原因として、左房内で形成されたフィブリン血栓が栓子として遊離し、血流に依存して脳動脈に流入、突如大きな脳血管を閉塞することで発症する。梗塞巣は広範にわたり脳浮腫を形成しやすく、生命予後を含め転帰不良例が多い。
また、心原性脳塞栓症における心房細動の合併率は72.8%3)といわれている(図1B)。一次予防として心房細動への介入は脳梗塞の抑制に貢献する。疫学的検討によれば、心房細動を早期検出し適切な用量調整を行った場合の抑制率はワルファリンで約6割、抗血小板で約2割4)と報告されている。心房細動は、脳梗塞の大きなリスクであると同時に予防効果の高いリスク因子でもある。わが国における心房細動の疫学あるいは臨床的特徴に関するデータは限定的であるが、心房細動患者の多施設共同実態調査5)では加齢に伴い有病率が上昇することが報告されており、心房細動の早期検出、早期介入の重要性はますます高まると考えられる。
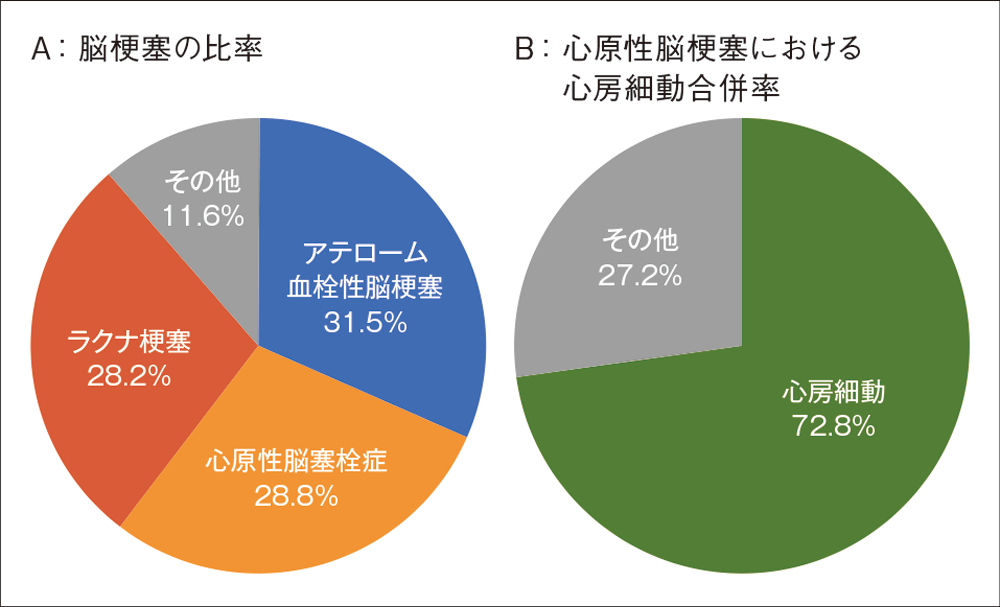
図1
脳梗塞の比率と心原性脳梗塞における心房細動の合併率
A:文献2)、B:文献3)より作図
心房細動の早期検出と脳梗塞の予防
現在、日本脳卒中協会と日本不整脈心電学会は3月9日を「脈の日」[3(みゃ)月9(く)日]と定め、広く国民に検脈の実施(図2)と心房細動の症状、脳梗塞の予防の必要性を啓発している6)。このイベントを通じ、心房細動の症状、脳梗塞の危険性と医学的管理の必要性を広く周知し、心房細動からの脳梗塞を予防すべく活動を展開している。
心房細動による脳梗塞の予防は、過去にはビタミンK拮抗薬であるワルファリンしか使用できなかったが、2011年以降、複数の直接阻害型経口抗凝固薬(direct oral anticoagulant : DOAC)が登場してきた。心房細動を対象とした大規模臨床試験のメタ解析によれば、DOAC全体としてワルファリンに比較し、脳卒中および全身性塞栓症、全死亡率、頭蓋内出血を有意に減少させ、大出血はワルファリンと同程度であったことが示されている7)。
DOACはワルファリンと違い、薬効のモニタリングが不要、食物や併用薬との相互作用が少ない、固定用量で投与可能、という特徴があり、臨床現場で広く用いられるようになっている。DOACの普及に伴い脳卒中の発症率が低下傾向に転じたという海外からの報告8)もあり、適切な心房細動管理によって脳梗塞を減らせるもの、と期待されている。
図2
検脈
脳卒中領域の新たな話題
1.高尿酸血症と心房細動
近年の数々の疫学調査とそれらのシステマティックレビュー、メタ解析から、血清尿酸値は心房細動の独立したリスク因子と考えられるようになった。
根拠の一つとして、心房細動モデルでの検討がある。左心房のキサンチン酸化酵素(XO)活性は有意に上昇しており、XO阻害薬であるoxypurinolを投与すると心房の活性酸素が減少した9)。同様にヒトの検討でも、心房細動患者の心房組織では活性酸素産生が増加していた10)ことから、XO活性が心房細動の病態に重要と推測されている。
また、尿酸そのものが局所ならびに循環レニン-アンギオテンシン系(RAS)を活性化して心房の炎症に関与する可能性11)が示されているほか、心房における尿酸トランスポーターURATv1を介して細胞内に尿酸が蓄積し、酸化ストレスの増加、ERKリン酸化を介して心房不応期短縮を起こし心房細動発症に関与する可能性12)も指摘されている。
しかし、これまで高尿酸血症への介入が心房細動の発症リスクを軽減できるかについての研究は行われていない。関連文献として、高尿酸血症を合併する心血管疾患ハイリスク患者に対してトピロキソスタットを投与したところ、脳性ナトリウム利尿ペプチド(BNP)や脳卒中のリスク因子とされるhs-CRPが有意に低下したという報告がある13)。今後、心房細動患者に対する尿酸ならびにXOを標的とした介入効果についての検討が期待される。
2.ESUS
近年の脳卒中領域におけるトピックは塞栓源不明脳塞栓症(embolic stroke of undetermined source : ESUS)である。いわゆる潜因性脳梗塞(cryptogenic stroke)のうち、先に述べた脳梗塞の3大病型やその他の原因疾患を除外した一群であり、塞栓性機序が想定される患者が多くを占める。
ESUSの原因として最も頻度が高く重要と考えられるのが、潜在性発作性心房細動である。これは通常の12誘導心電図やホルター心電図では検出されていないが、実際には発作性心房細動が潜在しており、脳塞栓症の原因となったという仮説に基づく。その根拠に、記録時間の長い植込み型や長時間心電図を用いた観察研究では、心房細動検出率が向上したという観察研究がある14)-16)。
発作性心房細動がESUSの主因だとすれば、再発予防には抗凝固療法が有効と考えられる。この仮説に基づき、これまでESUS患者においてDOACとアスピリンを比較する2件の大規模臨床試験が行われた。RE-SPECT ESUS試験はダビガトランをアスピリンと比較したが、塞栓症の再発に有意差は認められなかった17)。NAVIGATE ESUS試験ではリバーロキサンとアスピリンが比較されたが、塞栓症の再発に有意差は認められず、リバーロキサンで大出血が有意に多いという結果であった18)。
これらの結果から、『脳卒中治療ガイドライン2021〔改訂2023〕』は、ESUSと診断された場合はDOACではなくアスピリンを使用することが妥当とされている(推奨度B)1)。ただし、日本の非弁膜性心房細動における症候性脳梗塞のアスピリンによる予防効果に関する大規模調査研究JAST studyの結果からは、低用量アスピリンは心房細動に推奨されない19)。発作性心房細動が本当にESUSの主因であるならば、現在のガイドラインとは合致しないことになる。これを踏まえ、臨床の現場では、ESUSのなかでも抗凝固療法に反応性があると考えられる病態を可能な限り抽出し、個別化された治療(tailor made therapy)を実践する必要がある。
3.atrial cardiopathy
抗凝固療法に反応性のある病態として近年、atrial cardiopathyが注目されている。そもそも心房細動は血管性リスク因子などにより左房の心筋症性変化を生じ、電気的機能不全や線維化によって発症する。Atrial cardiopathyは心房細動の前段階という位置付けで、運動機能不全や凝固亢進状態によって心房細動を介することなく脳塞栓症を発症するという概念である。
そこで、ESUSのうちatrial cardiopathyを認める患者を対象としたARCADIA試験が行われた。本試験では、3つのバイオマーカーのPTFV1、左房径拡大、N末端プロ脳性ナトリウム利尿ペプチド(NT-proBNP)高値によってatrial cardiopathyを定義し、DOACとしてアピキサバンを選択、アスピリンと比較した。大きな期待を持って試験の進捗が見守られていたが、2023年5月の欧州脳卒中機構会議においてアピキサバンにアスピリンを上回る効果はなかったことが発表された20)。
あくまで私見であるが、ARCADIA試験で抗血小板作用を期待して使ったアスピリン(アセチルサリチル酸)は、古くからある消炎鎮痛剤でもある。抗炎症作用という観点でアスピリンにDOACを上回る効果があったのかもしれない。
さいごに
心原性脳塞栓症の多くは心房細動(潜在性発作性心房細動も含め)を要因としている。その予防には検脈による心房細動の早期発見が重要であり、医療機関の受診時のみならず、日頃から患者さんご自身で正しく検脈を行うことが大切である。また、その心房細動を引き起こす因子の1つとして血清尿酸値もリスクとして注目されているため、日頃からの尿酸管理の重要性も念頭に置きたい。心房細動の早期発見・早期治療介入により脳梗塞の発症を減らし、ひいては健康寿命の延伸につながることを期待したい。
References
1) 日本脳卒中学会 脳卒中ガイドライン委員会(編).脳卒中治療ガイドライン2021〔改訂2023〕.東京:協和企画;2023.
2) 豊田一則, 他. 国循脳卒中データバンク2021編集委員会(編).脳卒中データバンク2021.東京:中山書店;2021. p.20-7
3) 卜蔵浩和, 他. 小林祥泰(編). 脳卒中データバンク2015. 東京 : 中山書店 ; 2015. p.56-7.
4) Hart RG, et al. Ann Intern Med. 2007 ; 146 : 857-67.
5) Tomita F,et al.Jpn Circ J.2000;64:653-8.
6) 公益社団法人 日本脳卒中協会.心房細動週間・脈の日.http://www.jsa-web.org/citizen/94.html(閲覧:2023-9-15)
7) Ruff CT,et al.Lancet.2014;383:955-62.
8) Cowan JC, et al. Eur Heart J. 2018 ; 39 : 2975-83.
9) Dudley SC,et al.Circulation.2005;112:1266-73.
10) Korantzopoulos P,et al.Int J Cardiol.2007;115:135-43.
11) Mazzali M,et al.Hypertension.2001;38:1101-6.
12) Maharani N,et al.Circ J.2015;79:2659-68.
13) 九鬼新太郎,他.Ther Res.2016;37:49-57.
14) Higgins P,et al.Stroke.2013;44:2525-31.
15) Sanna T,et al.N Engl J Med.2014;370:2478-86.
16) Gladstone DJ,et al.N Engl J Med.2014;370:2467-77.
17) Diener HC,et al.N Engl J Med.2019;380:1906-17.
18) Hart RG,et al.N Engl J Med.2018;378:2191-201.
19) Sato H,et al.Stroke.2006;37:447-51.
20) Kamel H, et al. presented at ESOC 2023, Munich, Germany



